Médicaments et santé
Soins du corps et beauté
Nutrition et sport
Parents et enfants
Hygiène et traitement
Ménage
Promotions
8.50
Détails
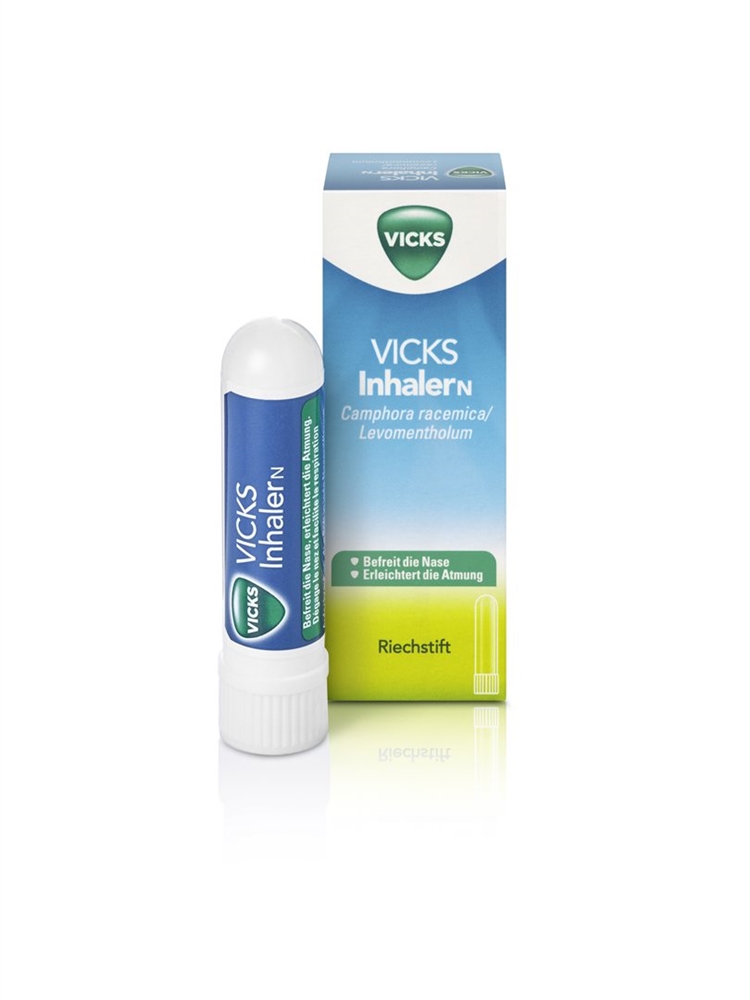
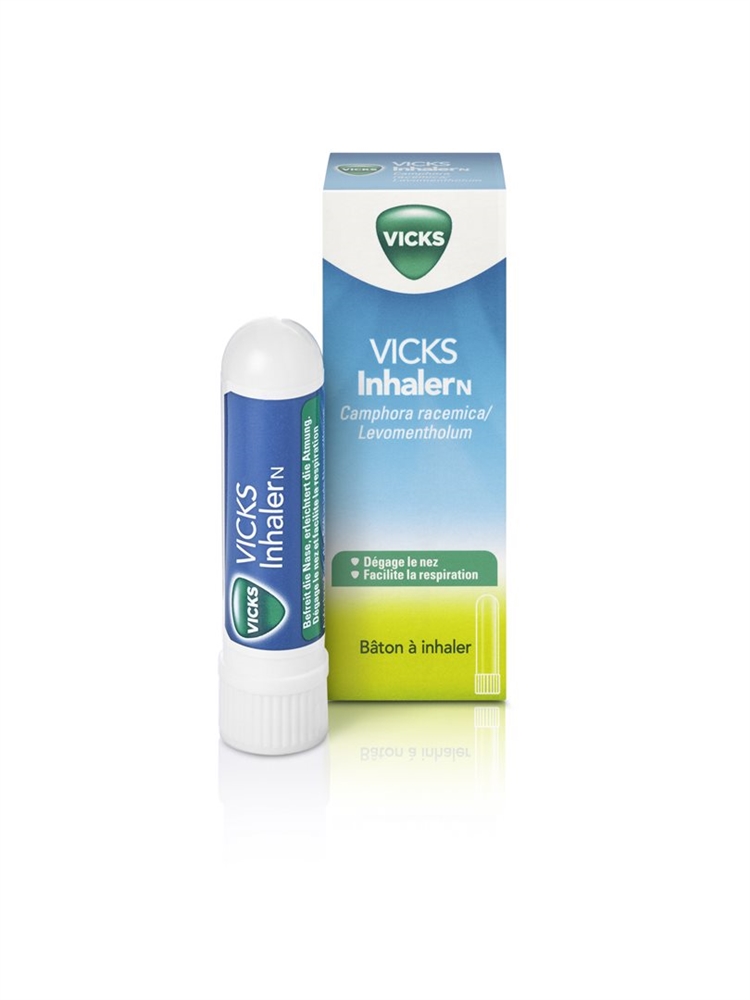
Soulage la respiration en cas de nez bouché
Les symptômes d’un refroidissement, tels que le nez bouché, peuvent être gênants. Le stick inhaler Vicks déploie son effet bienfaisant en libérant le nez, ce qui vous permet de respirer plus facilement. Pratique en déplacement.
Ceci est un médicament autorisé. Lisez la notice d’emballage. Procter & Gamble International Operations SA
Adultes: selon besoin plusieurs ×/j., tenir alternativement devant chaque narine et aspirer à fond tout en maintenant l'autre fermée; durée du traitement: max. 7 j. sans interruption.
Composition / principes actifs
41.54 % Camphre racémique
,
41.54 % Lévomenthol
,
Aromatica
,
Salicylate méthyle
,
Essence d' épicéa commun
Information destinée aux patients
Information patient approuvée par Swissmedic
Procter & Gamble International Operations SA
Vicks Inhaler N est un bâton à inhaler qui contient des substances soulageant la respiration en cas de nez bouché.
Ne pas utiliser chez les nourrissons et les enfants en bas âge de moins de 2 ans.
En cas d'hypersensibilité à l'un des constituants.
En cas d'asthme bronchique, de coqueluche, de pseudocroup et d'autres maladies respiratoires associées à une hypersensibilité prononcée des voies respiratoires.
L'inhalation de Vicks Inhaler N peut entraîner un rétrécissement des bronches.
Eviter le contact avec les yeux.
Veuillez informer votre médecin, votre pharmacien ou votre droguiste si
•vous souffrez d'une autre maladie
•vous êtes allergique
•vous prenez déjà d'autres médicaments ou utilisez déjà d'autres médicaments en usage externe (même en automédication!).
Vicks Inhaler N ne doit pas être utilisé pendant la grossesse et l'allaitement.
Adultes: avant usage bien se moucher, tenir le bâton à inhaler alternativement devant chaque narine. Aspirez à fond tout en maintenant l'autre narine fermée. Si nécessaire répétez plusieurs fois par jour.
L'utilisation et la sécurité de Vicks Inhaler N chez l'enfant et l'adolescent n'ont pas été vérifiées à ce jour. Ne pas utiliser pendant plus de 7 jours sans interruption.
Veuillez vous conformer au dosage figurant sur la notice d'emballage ou prescrit par votre médecin.
Si vous estimez que l'efficacité du médicament est trop faible ou au contraire trop forte, veuillez vous adresser à votre médecin, votre pharmacien ou votre droguiste.
Les principes actifs lévomenthol et camphre racémique peuvent provoquer des réactions d'hypersensibilité (y compris détresse respiratoire et un spasme du larynx). En cas de dyspnée, arrêtez le traitement et adressez-vous immédiatement à votre médecin.
Occasionnel (concerne 1 à 10 utilisateurs sur 1000)
Des irritations locales de la muqueuse nasale, un larmoiement.
Très rare (concerne moins d'un utilisateur sur 10'000)
Une sensation de brûlure et de piqûre dans le nez.
Fréquence inconnue (ne peut être estimée sur la base des données disponibles)
Des irritations cutanées, des eczémas de contact et d'autres hypersensibilités cutanées.
Consultez votre médecin si les symptômes persistent ou s'aggravent.
Si vous remarquez des effets secondaires, veuillez en informer votre médecin, votre pharmacien ou votre droguiste. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d'emballage.
Conserver hors de portée des enfants.
Conserver à température ambiante (15–25 °C).
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Pour de plus amples renseignements, consultez votre médecin, votre pharmacien ou votre droguiste, qui disposent d'une information détaillée destinée aux professionnels.
1 Vicks Inhaler N contient:
Principes actifs
Camphre 41.54 % m/m, lévomenthol 41.54 % m/m.
Excipients
Arômes: salicylate de méthyle, huile essentielle d'aiguilles de sapin de Sibérie.
13866 (Swissmedic).
En pharmacie et droguerie, sans ordonnance médicale.
Emballages de 1 bâton à inhaler.
Procter & Gamble International Operations SA, Lancy.
Domicile: 1213 Petit-Lancy.
Cette notice d'emballage a été vérifiée pour la dernière fois en juin 2024 par l'autorité de contrôle des médicaments (Swissmedic).
Numéro d’article
1747770